
Ce programme s’appuie sur l’expertise de 12 équipes de recherche dans des domaines variés (organoïdes, radiologie, bioinformatique, immunité macrophagique) et sur 9 infrastructures et plateformes partagées. Grâce à ces ressources et à l’équipement institutionnel de nos partenaires, nous visons à :
- Mieux comprendre et surmonter la résistance à la radiothérapie des tumeurs cérébrales pédiatriques,
- Proposer des thérapies innovantes,
- Faciliter leur transfert en pratique clinique.
Ce programme est structuré autour de quatre axes de recherche interdépendants :
Identification des altérations intrinsèques et extrinsèques caractérisant les cellules de tumeur cérébrale résistantes aux radiations.
- Développement de modèles 3D avancés dérivés de tumeurs cérébrales pédiatriques et mise au point d’une biobanque de modèles d’étude.
- Approches multi-omiques avancées, incluant des analyses unicellulaires et spatiales pour décrypter la radiorésistance.

Identification et validation de mécanismes clés de radiorésistance
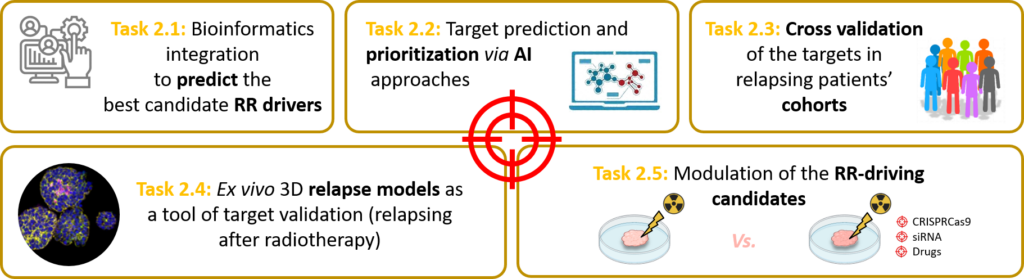
- Utilisation d’outils bioinformatiques pour identifier les mécanismes clés.
Développement d’approches thérapeutiques ciblant la radiorésistance dans des modèles ex vivo et in vivo.
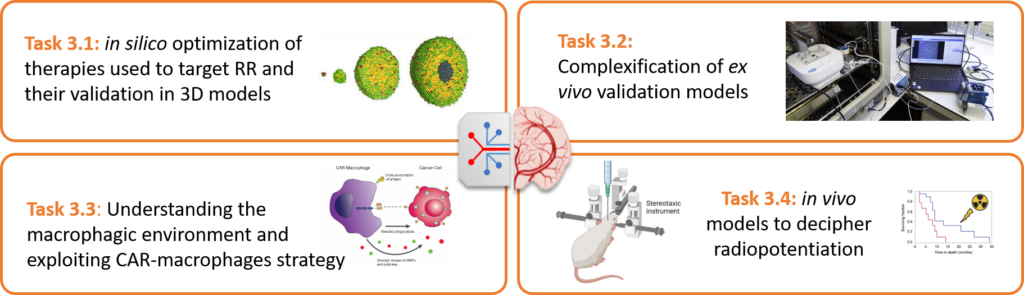
- Élaboration de traitements permettant de re-sensibiliser les cellules tumorales à la radiothérapie.
- Analyse des interactions entre les cellules tumorales et leur microenvironnement pour identifier les cibles thérapeutiques prometteuses.
- Exploration de nouvelles approches de radiopotentiation et notamment de l’immunothérapie macrophagique (CAR-macrophages).
Applications cliniques
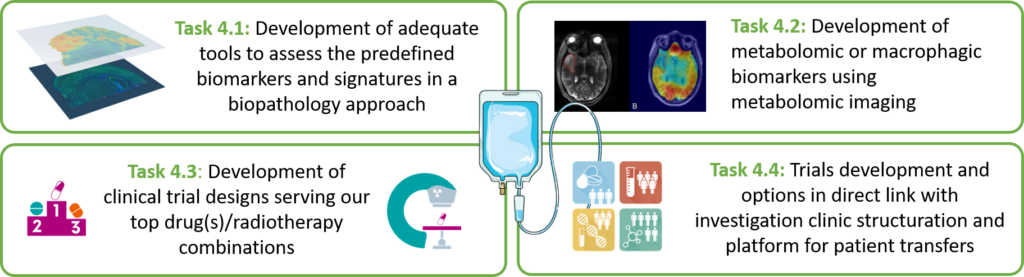
- Développement d’essais cliniques combinant radiothérapie et nouveaux traitements.
- Validation de l’utilisation de biomarqueurs et développement d’outils cliniques pour une meilleure personnalisation des traitements.
Publications scientifiques
2026
Profiler: an open web platform for multi-omics analysis.
Zirem Y., Ledoux L., Fournier I., Salzet M. Bioinformatics. 2026 Jan 2. doi: 10.1093/bioinformatics/btaf644.
2025
Novel Diffuse Midline Glioma-on-Chip Recapitulating Tumor Biophysical Microenvironment to Assess the Heterogeneity of Response to Therapies. Terrassoux, L., Hazard, C., Laratte, A., Balsamelli, J., Arcicasa, M., Fong, E., Baland, L., Soncin, F., Cappello, G., Maurage, C. A., Janel, S., Bazir, A., Cleri, F., Treizebre, A., Lartigau, E., Rekik, Y., Meignan, S., & Furlan, A. 2025 Sept 29. Small (Weinheim an der Bergstrasse, Germany), e05343. https://doi.org/10.1002/smll.202505343.
Challenging CDKN2A assessment in BRAF-altered gliomas: lessons from a pleomorphic xanthoastrocytoma-enriched cohort. Wolf T., Reita D., Deschuyter M., Salmanli C., Buffa J., Pencreach E., Guérin E., Jeandidier E., Miguet M., Chenard M. P., Geyer L., Noel G., Todeschi J., Gauchotte G., Martin S., Entz-Werlé N., & Lhermitte B. Acta Neuropathol Commun. 2025 Aug 11. doi: 10.1186/s40478-024-01901-w.
Internal ribosome entry sites enhance translation in trans in antisense non-coding SINEUP and circular RNAs.
Armirotti A., Scarpato M., Damiani D., Ros G., Di Carlo V., Maniscalco F., Bechara E., Tartaglia G. G., Carninci P., … Gustincich S. Nucleic Acids Res. 2025 Aug 11. doi: 10.1093/nar/gkae1151.
Nanopore sequencing as a cutting-edge technology for medulloblastoma classification.
Filser M., Torrejon J., Merchadou K., et al. Neuro-Oncology. 2025 Jun 21. doi: 10.1093/neuonc/noae279.
A structural element within the 5’UTR of β-catenin mRNA modulates its translation under hypoxia.
D’Agostino M., Rol-Moreno J., Bec G., Kuhn L., Ennifar E., Simonetti A. Nucleic Acids Res. 2025 Apr 22;53(8):gkaf321. doi: 10.1093/nar/gkaf321.
A coregulatory influence map of glioblastoma heterogeneity and plasticity.
Bernhard C., Geles K., Pawlak G., Dhifli W., Dispot A., Dusol J., Kondratova M., Martin S., Messé M., Reita D., Tulasne D., Van Seuningen I., Entz-Werle N., Ciafrè S. A., Dontenwill M., Elati M. Npj Precis Oncol. 2025 Apr 15;9(1):110. doi: 10.1038/s41698-025-00890-0.
CIC/ATXN1-rearranged tumors in the central nervous system are mainly represented by sarcomas: A comprehensive clinicopathological and epigenetic series. Tauziède-Espariat A., Ebrahimi A., Boddaert N., et al. Brain Pathol. 2025 Mar. doi: 10.1111/bpa.13327.
Predicting Protein Pathways Associated to Tumor Heterogeneity by Correlating Spatial Lipidomics and Proteomics: The Dry Proteomic Concept.
Lagache L., Zirem Y., Le Rhun É., Fournier I., Salzet M. Mol Cell Proteomics. 2025 Jan;24(1):100891. doi: 10.1016/j.mcpro.2024.100891.
2024
Inhibition of furin in CAR macrophages directs them toward a proinflammatory phenotype and enhances their antitumor activities.Ziane-Chaouche, L., Raffo-Romero, A., Hajjaji, N., Kobeissy, F., Pinheiro, D., Aboulouard, S., Cozzani, A., Mitra, S., Fournier, I., Cizkova, D., Salzet, M., & Duhamel, M. Cell death & disease. 2024 Dec 4;15(12), 879. https://doi.org/10.1038/s41419-024-07267-4.
Clinical impact of large genomic explorations at diagnosis in 198 pediatric solid tumors: a monocentric study aiming practical feasibility of precision oncology.
Simon J., Reita D., Guerin E., et al. BMC Cancer. 2024 Oct 21. doi: 10.1186/s12885-024-13034-7.
Overcoming the limits of pediatric brain tumor radiotherapy: The use of preclinical 3D models.
Czuba E., Deschuyter M., Entz-Werlé N., Noël G., Burckel H. Review Cancer Radiother. 2024 Oct;28(5):424-434. doi: 10.1016/j.canrad.2024.06.003.
A co-culture system of macrophages with breast cancer tumoroids to study cell interactions and therapeutic responses.
Raffo-Romero A., Ziane-Chaouche L., Salomé-Desnoulez S., Hajjaji N., Fournier I., Salzet M., Duhamel M. Cell Rep Methods. 2024 Jun 17;4(6):100792. doi: 10.1016/j.crmeth.2024.100792.
Real-time glioblastoma tumor microenvironment assessment by SpiderMass for improved patient management.
Zirem Y., Ledoux L., Roussel L., Maurage C. A., Tirilly P., Le Rhun É., Meresse B., Yagnik G., Lim M. J., Rothschild K. J., Duhamel M., Salzet M., Fournier I. Cell Rep Med. 2024 Apr 16;5(4):101482. doi: 10.1016/j.xcrm.2024.101482.
Mis à jour le 26/02/2026